Przewlekła choroba oskrzelowo-płucna jest najczęstszą manifestacją objawów występującą w mukowiscydozie. Mutacje genu CFTR skutkują zaleganiem gęstej treści w drogach oddechowych, co stanowi świetną pożywkę dla bakterii. Wcześnie, bo już w młodym wieku, pacjenci chorzy na mukowiscydozę borykają się z nawrotowymi infekcjami układu oddechowego, które z czasem przybierają charakter przewlekły. Przewlekłe zakażenie prowadzi do nieodwracalnego uszkodzenia płuc.
Kolonizacja, nosicielstwo, zakażenie
Kolonizacja to występowanie patogenów (niechorobotwórczych lub chorobotwórczych) na powierzchni nabłonka dróg oddechowych bez wywoływania stanu zapalnego. Nosicielstwo to stan równowagi immunologicznej, bytowanie patogenów chorobotwórczych, bez objawów zakażenia i bez odpowiedzi układu immunologicznego. Zakażenie jest natomiast definiowane jako obecność bakterii w drogach oddechowych, które wywołują objawy choroby (gorączkę, zwiększenie ilości gęstej wydzieliny, nasilenie produktywnego kaszlu, objawy bólowe ze strony gardła i zatok).
Mikrobiom. Naturalna flora górnych dróg oddechowych.
Żyjemy wśród bakterii. Szacuje się, że liczba bakterii bytujących w i na człowieku dziecięciokrotnie przewyższa liczbę komórek, z których zbudowany jest ludzki organizm. Powszechne jest występowanie drobnoustrojów we wszystkich układach, w tym w układzie oddechowym. U zdrowych ludzi zróżnicowanie tych drobnoustrojów jest ogromne. Do bakterii fizjologicznie zasiedlających w znacznej liczbie błony śluzowe górnych dróg oddechowych zaliczamy między innymi: Streptococcus viridans, Moraxella catarrhalis, Staphylococcus epidermidis, Streptococcus salivarius. Wymienione drobnoustroje nie stanowią zagrożenia dla pacjentów z mukowiscydozą i zwykle nie wymagają wdrożenia leczenia.
Mikrobiom człowieka to całościowe określenie środowiska złożonego z drobnoustrojów zasiedlających ludzki organizm, tworzących barierę ochronną, symbiotycznych i chorobotwórczych. Zamieszkiwanie organizmu człowieka przez bakterie, które komunikują się ze sobą nawzajem, a także z komórkami gospodarza, odgrywa ważną rolę w procesach decydujących o zdrowiu i chorobie. To zagadnienie jest stopniowo coraz lepiej poznawane.
Metody diagnozowania
W diagnostyce mikrobiomu układu oddechowego dużą rolę odgrywają metody genotypowania mikroorganizmów, jednak w codziennej praktyce klinicznej częściej korzysta się z konwencjonalnych badań mikrobiologicznych. Badanie mikrobiologiczne to proces wieloetapowy, składa się z pobrania materiału, jego posiewu, hodowli, oceny mikroskopowej, ustalenia antybiogramu i klasyfikacji drobnoustroju.
Posiew plwociny z dolnych dróg oddechowych ze względu na dużą dostępność, niski koszt i powszechnie akceptowany sposób uzykania materiału stanowi najlepsze źródło informacji o florze patogennej i drobnoustrojach kolonizujących układ oddechowy. Służy do monitorowania zaawansowania choroby, a także wykrywania nowych gatunków, dzięki czemu możliwe jest szybkie wdrożenie celowanej antybiotykoterapii (według antybiogramu). Dlatego tak ważne jest regularne badanie plwociny. Materiał uzyskuje się poprzez samoczynne odkrztuszenie treści oskrzelowej, indukcję odkrztuszenia plwociny solą hipertoniczną (po wcześniejszym podaniu bronchodilatatora) lub poprzez odessanie treści w trakcie bronchoskopii. U pacjentów z mukowiscydozą zaleca się kontrolne badanie plwociny co 3–6 miesięcy. Wymazy z nosogardła są mało przydatne, ponieważ nie dostarczają informacji o florze dolnych dróg oddechowych, tak ważnych zwłaszcza w przypadku zakażenia Pseudomonas aeruginosa. W praktyce klinicznej nie stosuje się także badań serologicznych, które mają ograniczoną czułość w wykrywaniu wczesnego zakażenia pałeczką ropy błękitnej, są też trudno dostępne. Obiecujące wydają się doniesienia nt. wykrywania zakażeń Pseudomonas aeruginosa za pomocą „elektronicznego nosa” bazującego na nieinwazyjnej technologii macierzy z chemoczujnikami badającymi obecność patogenów w powietrzu wydychanym.
Zakażenia bakteryjne
U osób zdrowych i u chorych na mukowiscydozę inne czynniki etiologiczne odgrywają rolę w zakażeniach bakteryjnych układu oddechowego. Zakażenia dolnych dróg oddechowych u pacjentów nie chorujących na mukowiscydozę najczęściej są wywołane przez Streptococcus pneumoniae, rzadziej Haemophilus influenzae, bakterie atypowe, bardzo rzadko przez Staphylococcus aureus i pałeczki Gram (-). U chorych na mukowiscydozę początkowo przyczyną zakażeń są bakterie pochodzące ze środowiska człowieka: pałeczka grypy – Haemophilus influenzae, gronkowiec złocisty – Staphylococcus aureus, a nastepnie, co wiąże się z progresją choroby – zakażenie Pseudomonas aeruginosa, bakterie oportunistyczne i inne pałeczki Gram (-)1. Zdrowi pacjenci, bez zaburzeń odporności, nie są narażeni na zakażenie patogenami, które najczęściej występują u chorych na mukowiscydozę, dlatego też całkowicie bezpieczne są hospitalizacje immunokompetentnych pacjentów w jednej sali z chorymi na CF.
Staphylococcus aureus – to patogen obecny w środowisku człowieka, będący częstą przyczyną kolonizacji nabłonka dróg oddechowych u ludzi zdrowych (ok. 30% zdrowych dzieci). Najwcześniej zasiedla układ oddechowy chorych na mukowiscydozę. Jego obecność stwierdzano już u 3-miesięcznych niemowląt. Podaje się, że ok. 60% chorych na mukowiscydozę jest przewlekle zakażonych gronkowcem złocistym. Bakteria przenosi się drogą kropelkową, przez kontakt bezpośredni, a także przez przedmioty codziennego użytku. Wyróżniamy szeczepy wrażliwe na metycylinę – MSSA (methicillin-sensitive Staphylococcus aureus) oraz oporne na metycylinę – MRSA (methicyllin resistant Staphylococcus aureus). Pojawienie się oporności na metycylinę, a tym samym na wszystkie antybiotyki betalaktamowe, wiąże się z cięższym przebiegiem choroby, przyspieszeniem tempa spadku wskaźników spirometrycznych oraz skróceniem długości życia.
![Bakteria Staphylococcus aureus pod mikroskopem elektronowym Autorzy: Eric Erbe, Christopher Pooley [Public domain], Wikimedia Commons](https://infomuko.ptwm.org.pl/wp-content/uploads/2018/07/m52-rola_zakazen_2-808x1024.jpg)
Autorzy: Eric Erbe, Christopher Pooley [Public domain],
Wikimedia Commons
Haemophilus influenzae – nazywana potocznie pałeczką grypy, jest bakterią Gramujemną przenoszącą się wyłącznie z człowieka na człowieka drogą kropelkową lub przez bezpośredni kontakt z wydalinami lub wydzielinami. Jest częstą przyczyną kolonizacji błon śluzowych, może także powodować objawy ze strony górnych i dolnych dróg oddechowych, w tym zagrażające życiu zapalenie nagłośni, zapalenie opon mózgowo-rdzeniowych, szpiku kostnego, stawów, osierdzia, tkanki łącznej oczodołu, gałki ocznej oraz układu moczowego. Na zakażenie najbardziej podatne są dzieci do 2 r.ż., u których stwierdza się niski poziom przeciwciał nabytych od matki. W mukowiscydozie częściej jest izolowana u dzieci niż u dorosłych. W Polsce w obowiązkowym kalendarzu szczepień uwzględniono szczepienia przeciw Haemophilus influenzae w 4-dawkowym schemacie szczepienia.
![Haemophilus influenzae Autor: Manurx27 [CC BY-SA 4.0 (https://creativecommons.org/ licenses/by-sa/4.0)], Wikimedia Commons](https://infomuko.ptwm.org.pl/wp-content/uploads/2018/07/m52-rola_zakazen_1-1024x768.jpg)
Autor: Manurx27 [CC BY-SA 4.0 (https://creativecommons.org/licenses/by-sa/4.0)],
Wikimedia Commons
Pseudomonas aeruginosa, czyli pałeczka ropy błękitnej występująca głównie w glebie, wilgotnym środowisku, a także na powierzchni roślin. Jest przyczyną zakażeń oportunistycznych – tzn. dotyczy osób z obniżoną odpornością oraz zakażeń wewnątrzszpitalnych. To patogen najczęściej izolowany z treści oskrzelowej chorych na mukowiscydozę (blisko 80% chorych dorosłych i ok. 25% dzieci). Poszczególne szczepy różnią się między sobą zjadliwością i lekoopornością. Szczepy epidemiczne mogą przenosić się pomiędzy chorymi, dlatego tak ważna jest izolacja pacjentów przebywających w oddziałach szpitalnych. W zakażeniu Pseudomonas aeruginosa udowodniono także torującą rolę infekcji wirusowych.
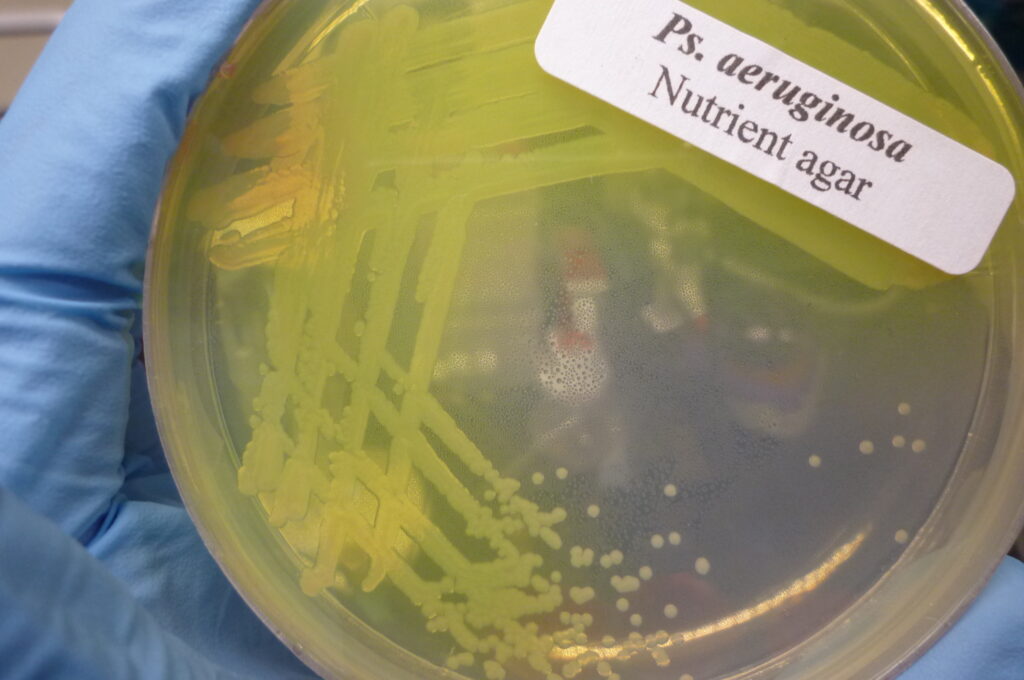
Autor: Sun14916 [CC BY-SA 3.0 (https://creativecommons.org/licenses/by-sa/3.0)],
Wikimedia Commons
Bakteria zaopatrzona jest w pojedynczą rzęskę, dzięki której z łatwością przenika przez warstwę gęstego śluzu. Dzięki właściwościom adhezyjnym, wytwarzaniu proteaz i zdolności szybkiej adaptacji do zmian otoczenia zasiedla błony śluzowe, rozmnaża się w warunkach utrudnionego dostępu do tlenu i ogranicza penetrację antybiotyków do miejsca zakażenia.
Zakażenie pałeczką ropy błękitnej wiąże się z pogorszeniem stanu klinicznego, zwiększeniem częstotliwości zaostrzeń, liczby hospitalizacji, pogorszeniem wskaźników spirometrycznych. Przewlekłe zakażenie Pseudomonas aeruginosa stwierdzane jest wówczas, kiedy w co najmniej połowie posiewów plwociny wykonanych w ciągu 12 miesięcy wykryty został patogen. Ryzyko przewlekłego zakażenia jest większe u płci żeńskiej, osób niedożywionych, często hospitalizowanych, z gorszą funkcją układu oddechowego, u osób nieprzestrzegających zasad izolacji, u homozygot F508del/F508del. Po pierwszorazowym wykryciu Pseudomonas aeruginosa konieczne jest intensywne leczenie zmierzające do eradykacji i zapobieganiu przejścia w postać przewlekłą. W momencie pierwszej izolacji patogen udaje się wyeradykować w ok. 80% przypadków. W momencie przejścia w zakażenie przewlekłe, Pseudomonas aeruginosa wystepuje w postaci biofilmu wyjatkowo opornego na antybiotyki.
Burkholderia cepacia complex (BBC) – bakteria Gramujemna, występująca powszechnie w wilgotnym środowisku: gleba, przy korzeniach roślin (ściśle wiązana z procesem gnicia cebuli), a także stanowiąca groźny czynnik zakażeń szpitalnych (zdolność przetrwania nawet w środkach dezynfekcyjnych). W skład Burholderia cepacia complex wchodzi 17 szczepów. Stanowią duże zagrożenie nie tylko dla chorych na mukowiscydozę, ale także dla pacjentów z niedoborami immunologicznymi. Wśród pacjentów z CF najbardziej rozpowszechnione są zakażenia Burkholderia multivorans i Burkholderia cenocepacia (odpowiednio genomowar II i III), stanowiąc ok. 70% spośród wszystkich zakażeń BBC. Dzięki specyficznej budowie – nietypowe liposacharydy wchodzące w skład ściany komórkowej, BBC są jednymi z najbardziej opornych na antybiotyki patogenami, dodatkowo indukują odpowiedź zapalną w układzie oddechowym. Zakażenie gatunkami o większej zjadliwości wiąże się z groźnymi powikłaniami ze strony układu oddechowego, tj. szybką progresją choroby oskrzelowo-płucnej oraz martwiczym zapaleniem płuc, a także bakteriemią i w ciężkich przypadkach – posocznicą. Niektóre gatunki mogą przenosić się bezpośrednio pomiędzy chorymi, dlatego tak ważna jest izolacja i zakaz bezpośrednich kontaktów twarzą w twarz pacjentów z mukowiscydozą.

Autor: CDC/Janice Carr, Content Providers:
CDC/Janice Carr [Public domain],
Wikimedia Commons
Inne – rzadsze patogeny
Stenotrophomonas maltophilia – Gram ujemna bakteria występująca powszechnie w środowisku wilgotnym (gleba, ścieki, woda), a także na powierzchni roślin i w kale zwierząt. To patogen o niskiej zjadliwości stanowiący duże ryzyko zakażeń wewnątrzszpitalnych dla pacjentów z obniżoną odpornością. U chorych z mukowiscydozą infekcje Stenotrophomonas maltophilia stanowią ok. 20%. To bakteria o wysokiej oporności na stosowane antybiotyki. Prawdopodobnie nie przenosi się pomiędzy chorymi i nie powoduje przyspieszenia tempa spadku wskaźników oddechowych. Zaawansowanie zmian chorobowych, starszy wiek, płeć żeńska, liczne hospitalizacje i antybiotykoterapie zwiększają ryzyko zakażenia.
Achromobacter xylosoxidans to Gram ujemna bakteria oportunistyczna o niskiej zjadliwości, bytująca w środowisku wilgotnym. Stanowi także czynnik zakażeń szpitalnych. Cechuje ją wieloleko-oporność. Jest przyczyną bakteriemii, zapaleń płuc, opon mózgowo-rdzeniowych, układu moczowego, zapalenia wsierdzia, otrzewnej, zapalenia szpiku. U pacjentów z mukowiscydozą wykrywana jest stosunkowo rzadko (ok 10% chorych). Może przenosić się pomiędzy chorymi, dlatego ważne jest przestrzeganie zasad izolacji. Wykrycie Achromobacter w plwocinie chorego nie wiąże się z przyspieszeniem tempa zmian w układzie oddechowym.

Autor: CDC/ Dr. Rodney M. Donlan/ Janice Haney Carr (http://phil.cdc.gov/ ID#10548)
[Public domain], Wikimedia Commons
Gruźlica płuc i zakażenie prątkami niegruźliczymi są rzadkie w mukowiscydozie. Diagnostyka w kierunku Mycobacterium jest wskazana przy ujemnych wynikach hodowli plwociny u chorych z częstymi zaostrzeniami lub pogorszeniem stanu klinicznego. Wśród nontuber-culous mycobacteria (NTM) najczęściej spotykany jest M. avium complex. Czynniki ryzyka zakażenia to starszy wiek, niski status socjoekonomiczny, częste antybiotykoterapie, cukrzyca, leczenie glikokortykosteroidami, alergiczna aspergilloza oskrzelowo-płucna. Wśród pacjentów, u których wyizolowano z plwociny NTM, częstsze było przewlekłe zakażenie Staphylococcus aureus, rzadziej natomiast stwierdzano zakażenie Pseudomonas aeruginosa.
Zakażenia grzybicze
Oprócz zakażeń bakteryjnych w zaawanowanych stadiach mukowiscydozy pojawiają się zakażenia grzybicze. Wykazano, że kolonizacja dróg oddechowych grzybami u chorych na mukowiscydozę może być związana z progresją choroby, częstą antybiotykoterapią o szerokim spektrum, sterydoterapią systemową, cukrzycą, uszkodzeniem mechanicznym nabłonka dróg oddechowych, zaburzeniem funkcji wątroby, a także polekową neutropenią. Do najczęstszych zaliczamy Candida spp. i Aspergillus spp. Inne infekcje grzybicze dotyczą 8,6% pacjentów i obejmują Scedosporium apiospermum, Wangiella dermatitidis i Penicillium emersonii.
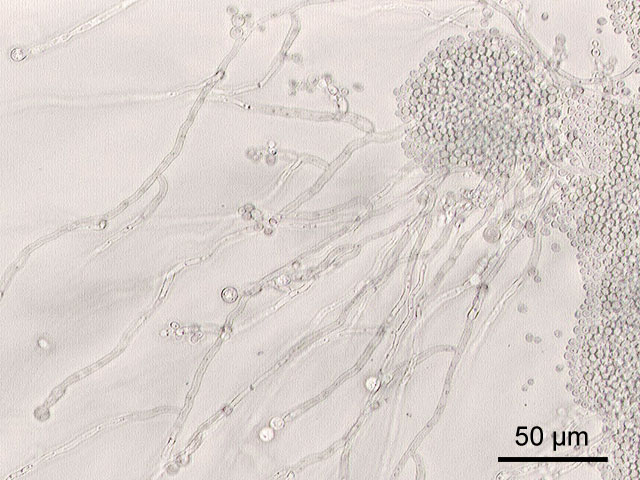
Autor: Y tambe (Y tambe’s file) [GFDL (http://www.gnu.org/copyleft/fdl.html) or CC-BY- -SA-3.0 (http://creativecommons.org/licenses/by-sa/3.0/)],
Wikimedia Commons
Rola zakażeń wirusowych
Zakażenia wirusowe często powodują zaostrzenie objawów choroby oskrzelowo-płucnej, przebieg infekcji u chorych na mukowiscydozę w przypadku dodatkowego zakażenia wirusowego jest zazwyczaj dłuższy. Najczęściej wykrywanym wirusem u małych dzieci jest RSV, następnie wirusy grypy, paragrypy i adenowirusy. Częstotliwość infekcji ma związek z sezonowością i jest podobna zarówno u pacjentów z CF, jak i osób zdrowych. Istnieją doniesienia, że wirusy i bakterie u pacjentów z mukowiscydozą wykazują działanie synergistyczne, prowadząc do promocji kolonizacji błon śluzowych dróg oddechowych przez bakterie patogenne. Opisywano również interakcje wirusów z komórkami nabłonka chorych z CF wywierające efekt prozapalny, najprawdopodobniej poprzez ułatwianie rozprzestrzeniania się bakterii z biofilmów w świetle dróg oddechowych.
Transmisja zakażenia pomiędzy chorymi
Ryzyko przeniesienia zakażenia bakteryjnego jest duże w przypadku Burkholderia cepacia, Pseudomonas aeruginosa, MRSA oraz wirusów oddechowych. Prawdopodobieństwo przeniesienia zakażenia jest tym większe, im kontakt pomiędzy chorymi jest bliższy i bardziej intensywny. Największe stężenie drobnoustrojów patogennych wykryto w otoczeniu chorego rano, bezpośrednio po wstaniu z łóżka, oraz po fizjoterapii. Przeniesienie zakażenia może odbywać się nie tylko na drodze powietrznopochodnej, ale także pośrednio przez podanie ręki, używanie wspólnych mydeł czy przyborów łazienkowych. Dlatego chorzy nie tylko w życiu codziennym, ale zwłaszcza w trakcie hospitalizacji bezwzględnie są zobowiązani do przestrzegania zasad izolacji.
Zakażenia układu oddechowego mają niewątpliwy wpływ na jakość i długość życia pacjentów z mukowiscydozą. Dzięki aktualnie stosowanym zasadom antybioterapii celowanej według antybiogramu, leczeniu mukolitykami, systematycznie prowadzonej fizjoterapii układu oddechowego możemy wpływać na przebieg zakażeń, a tym samym poprawiać komfort życia pacjentów. W procesie terapeutycznym istotną rolę odgrywa współpraca nie tylko z samym chorym, który powinien stosować się do zaleceń lekarskich, ale także z diagnostami laboratoryjnymi i fizjoterapeutami.
Bibliografia
- Binek M. Mikrobiom człowieka – zdrowie i choroba. Post. mikrobiol., 2012, 51, 1, 27–36.
- Gautam V., Singhal L., Ray P. Burkholderia cepacia complex: beyond pseudomonas and acinetobacter, Indian J Med Microbiol., 2011 Jan–Mar, 29(1): 4–12. doi: 10.4103/0255-0857.76516.
- Lipuma J.J. The Changing Microbial Epidemiology in Cystic Fibrosis, Clinical Microbiology Reviews, 2010, 23(2): 299–323. doi:10.1128/CMR.00068-09.
- Mazurek H. (red.) (2012), Mukowiscydoza, Medical Tribune Polska.
- Piorunek T., Cofta S., Goździk J., Batura-Gabryel H. Przewlekła kolonizacja drzewa oskrzelowego u dorosłych chorych na mukowiscydozę, Anestezjologia i Ratownictwo, 2011, 5: 11–16.
- Suarez-Cuartin G., Giner J., Merino J.L., Rodrigo-Troy-ano A., Feliu A., Perea L., Sanchez-Reus F., Castillo D., Plaza V., Chalmers J.D., Sibila O. Identification of Pseudomonas aeruginosa and airway bacterial colonization by an electronic nose in bronchiectasis, Respiratory Medicine 136, 2018, 111–117.