Pandemia COVID-19 spowodowana wirusem SARS-CoV-2 wywarła ogromny wpływ na naszą codzienność, modyfikując w zasadzie każdą sferę życia – pracę, edukację, kontakty społeczne, sposób spędzania wolnego czasu. Zastosowanie rygorystycznych obostrzeń nie zapobiegło, niestety, szerzeniu się pandemii nowego koronawirusa. Wiele osób doświadczyło ciężkich powikłań lub zmarło w związku z zakażeniem wirusem SARS-CoV-2 oraz w związku z przeciążeniem systemu opieki medycznej. Dodatkowo, mimo wielu nadziei pokładanych w różnych strategiach leczenia, w dalszym ciągu nie znaleziono skutecznego leku przeciwko chorobie COVID-19. Po ponad roku od początku pandemii nadal nie dysponujemy lekami przyczynowymi, a jedynie terapią objawową mającą na celu wspieranie układu odpornościowego w walce z infekcją. Nadzieję w walce z nowym koronawirusem pokładano w szybkim opracowaniu skutecznych i bezpiecznych szczepionek. Dzięki możliwości szczepienia mamy obecnie szansę uzyskania kontroli nad szerzeniem się wirusa SARS-CoV-2 oraz stopniowego powrotu do życia sprzed pandemii. Ale żeby to było możliwe, odporność musi nabyć większość osób w populacji.
Szczepienia ochronne są powszechnie znanym, bezpiecznym sposobem zapobiegania chorobom. Są jednym z największych osiągnięć medycyny, które uratowało życie milionom ludzi. Przyczyniły się one do eradykacji (wyeliminowania) wielu chorób zakaźnych charakteryzujących się wysoką śmiertelnością i ryzykiem ciężkich powikłań, takich jak ospa prawdziwa czy polio.
Zalecenia Polskiego Towarzystwa Mukowiscydozy
Zgodnie ze stanowiskiem Polskiego Towarzystwa Mukowiscydozy, szczepienie przeciwko COVID-19 należy rozważyć każdego chorego na mukowiscydozę. Poniżej przedstawiono najważniejsze wstępne zalecenia PTM (https://pcfs.pl/wp-content/uploads/2021/02/stanowisko-PTM-2.pdf ).
COVID-19 a mukowiscydoza
Z dotychczasowych danych wynika, że każda infekcja, która może prowadzić do uszkodzenia płuc, stanowi potencjalne ryzyko dla pacjentów z mukowiscydozą, zwłaszcza w zaawansowanym stadium choroby oskrzelowo-płucnej. Obecnie dysponujemy jedynie niewielką liczbą danych odnośnie przebiegu COVID-19 u chorych na mukowiscydozę. Według danych z Europejskiego Rejestru Chorych na Mukowiscydozę (EC-FSPR – European Cystic Fibrosis Society Patient Registry) na dzień 20.01.2021 r. zgłoszonych do rejestru chorych, u których rozpoznano COVID-19, było 851, z czego u 414 potwierdzono zakażenie wirusem SARS-CoV-2. Spośród osób z potwierdzonym zakażeniem 246 było bezobjawowych, 114 pacjentów było hospitalizowanych, w tym 17 w Oddziale Intensywnej Terapii, a 6 wymagało wentylacji mechanicznej, 7 osób zmarło.
| Stanowisko Polskiego Towarzystwa Mukowiscydozy – podsumowanie rekomendacji |
|---|
| Mukowiscydoza nie stanowi przeciwwskazania do szczepienia przeciwko wirusowi SARS-CoV-2. |
| Należy rozważyć szczepienie u każdego chorego na mukowiscydozę, także u osób, które przechorowały COVID-19. |
| Leczenie immunomodulujące stosowane u chorych po przeszczepieniu narządów oraz steroidoterapia przewlekła nie stanowią przeciwwskazań do szczepienia przeciwko COVID-19. |
| Jedynym bezwzględnym przeciwwskazaniem do szczepienia przeciwko COVID-19 jest ogólnoustrojowa reakcja anafilaktyczna po pierwszej dawce szczepionki lub przebyta ogólnoustrojowa reakcja anafilaktyczna na substancje wchodzące w skład szczepionki. |
| Przeciwwskazaniem czasowym do szczepienia jest zaostrzenie choroby oskrzelowo-płucnej lub inna ostra infekcja przebiegająca z gorączką, a także aktywne zakażenie wirusem SARS-CoV-2. |
Szczepienia przeciwko COVID-19
Zgodnie z aktualną rejestracją dostępnych w Europie szczepionek przeciw-ko COVID-19 możliwe jest szczepienie osób w wieku 16. lat i starszych (Pfizer/BioNTech) oraz 18. lat i starszych (Mo-derna, AstraZeneca). Niestety, nie opublikowano do tej pory danych z badań klinicznych odnośnie skuteczności i bezpieczeństwa szczepionek przeciwko COVID-19 w populacji pediatrycznej, ale w badaniach tych brały udział także dzieci w wieku 12. lat i starsze. Należy sądzić, że z czasem prawdopodobnie szczepienie będzie możliwe także w młodszych grupach wiekowych.
Aktualnie według Narodowego Programu Szczepień w grupie I znalazły się osoby poddawane przewlekłej wentylacji mechanicznej i po przeszczepieniu komórek, tkanek i narządów, u których stosuje się leczenie immunosupresyjne (w wieku 18. lat i więcej). Pozostali pełnoletni chorzy na mukowiscydozę znaleźli się, niestety, dopiero w III grupie (szczepienie pozostałej części populacji). W chwili obecnej nie jest znany termin rozpoczęcia szczepień w tych grupach, w programie szczepień nie uwzględniono dzieci w wieku 16. lat i starszych. Mimo to już teraz można zgłosić chęć zaszczepienia się. Można to zrobić za pośrednictwem Internetowego Konta Pacjenta (na stronie www.pacjent.gov.pl) lub poprzez formularz na stronie internetowej www.gov.pl/web/szczepimysie. Osoby, które wypełnią zgłoszenie, otrzymają informację o rozpoczęciu szczepień w ich grupie. Rejestracja na szczepienie będzie możliwa po rozpoczęciu szczepień w grupie, do której przypisana jest dana osoba. Wówczas na Internetowym Koncie Pacjenta pojawi się e-skierowanie na szczepienie, co umożliwi zapisanie się na konkretny termin do konkretnej placówki. Rejestracja będzie możliwa na kilka sposobów:
- przez bezpłatną Infolinię Narodowego Programu Szczepień – tel. 989,
- przez e-rejestrację na Internetowym Koncie Pacjenta (www.pacjent.gov.pl),
- bezpośrednio w wybranym przez siebie punkcie szczepień (wyszukiwarka punktów szczepień znajduje się na stronie https://www.gov.pl/web/szczepimysie/mapa-punktow-szczepien#/).
Podczas rejestracji nie ma konieczności podawania numeru e-skierowania na szczepienie. Po dokonaniu rezerwacji wizyty, każda osoba otrzyma SMS z informacją o wybranym miejscu i terminie szczepienia oraz ponowne powiadomienie dzień przed wizytą. Pacjent będzie od razu umawiany na 2 wizyty i także przed drugą dawką szczepionki otrzyma powiadomienie SMS.
Aktualnie punktami szczepień są przede wszystkim poradnie Podstawowej Opieki Zdrowotnej, ale także niektóre prywatne placówki opieki zdrowotnej i szpitale. Ze względów logistycznych obecnie nie jest możliwe przeprowadzenie szczepień w ośrodkach leczenia mukowiscydozy.
Na dzień dzisiejszy w Polsce zarejestrowane są szczepionki przeciwko COVID-19:
- Comirnaty Pfizer/BioNTech,
- Moderna COVID-19 Vaccine,
- COVID-19 Vaccine AstraZeneca.
Szczepionki te zostały przebadane w randomizowanych badaniach klinicznych i warunkowo dopuszczone do obrotu na etapie badań klinicznych fazy III, z uwagi na wysoką skuteczność i dobry profil bezpieczeństwa. Również po dopuszczeniu szczepionek do obrotu ich bezpieczeństwo będzie nadal ściśle monitorowane zgodnie z obowiązującymi normami prawnymi (badania kliniczne IV fazy).
Szczepionki Comirnaty Pfizer/BioNTech i Moderna Covid-19 Vaccine wykazują podobny, wysoki stopień skuteczności przeciwko zachorowaniu na COVID-19 (odpowiednio: 94,6% i 93,6%) przy dobrym profilu bezpieczeństwa. Oba preparaty należą do grupy tzw. szczepionek mRNA.
Szczepionki mRNA
Cząsteczka mRNA, czyli tzw. matrycowy kwas rybonukleinowy, jest formą zapisu informacji niezbędną do syntezy białek. W przypadku szczepionek przeciwko wirusowi SARS-CoV-2 zastosowano cząsteczkę mRNA kodującą fragment białka S wirusa (od ang. spike, tak zwane „białko kolca”). To struktura zlokalizowana na po-wierzchni wirusa SARS-CoV-2, niezbędna do tego, aby wirus mógł wniknąć do wnętrza komórki. Jest to zatem białko kluczowe dla przetrwania wirusa w organizmie człowieka i jego namnażania. Dla człowieka natomiast, jak każdy eksponowany na powierzchni fragment wirusa, jest ono czynnikiem uruchamiającym mechanizmy odporności, zarówno swoistej (prowadzącej do wytworzenia swoistych przeciwciał), jak i nieswoistej (tzw. odporności komórkowej).
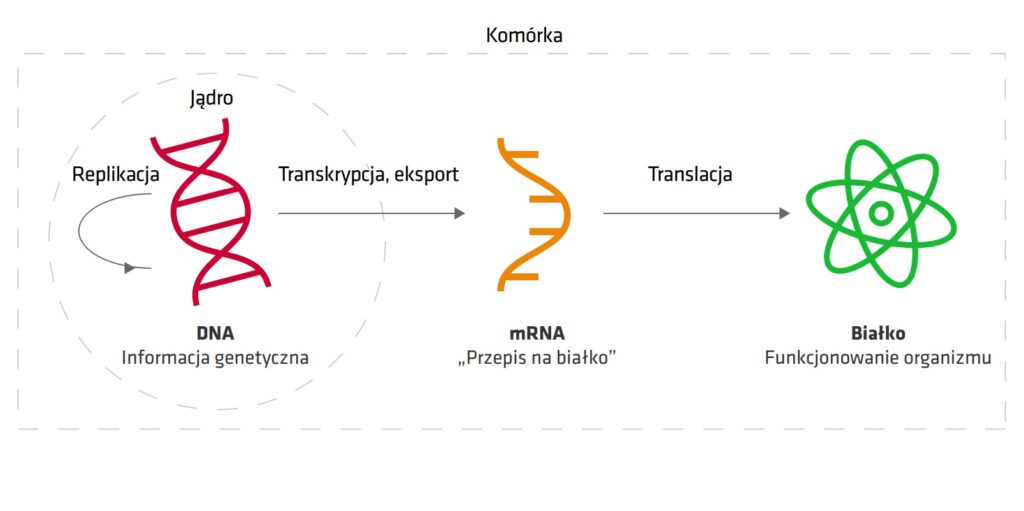
Aby łatwiej zrozumieć mechanizm działania tej szczepionki, warto przypomnieć sobie, jak dochodzi do produkcji białek w organizmie człowieka (rys. 1). W komórkach eukariotycznych (m.in. człowieka, roślin, zwierząt) informacja genetyczna kodująca białka znajduje się w jądrze komórkowym na łańcuchach DNA. DNA jako takie nie może opuścić jądra komórkowego i jest tam przechowywane niczym dane w archiwum. Aby powstało białko, gen (czyli fragment sekwencji DNA dla interesującego nas białka) przepisywany zostaje na sekwencję mRNA, która, dzięki nieco innej budowie, może opuścić jądro komórkowe. Zatem możemy sobie wyobrazić, że DNA jest „przepisem na białko” zapisanym na komputerze, a mRNA to wydruk przepisu. I tak jak nie da się włożyć kartki do komputera, tak nie ma możliwości, aby mRNA powróciło do jądra komórkowego, a także mRNA (u człowieka) nie może być przepisane na DNA (pod tym względem komputer, który potrafi odczytać tekst z kartki, jest od nas mądrzejszy). Gdy mRNA opuści jądro komórkowe, trafia do cytoplazmy komórki, gdzie zachodzi proces translacji, czyli odczytania przepisu i produkcji na jego podstawie białka. Z jednej cząsteczki mRNA może powstać wiele identycznych białek, tak jak z jednego przepisu wielokrotnie można upiec to samo ciasto. mRNA jest cząsteczką z na-tury bardzo niestabilną, po zakończeniu produkcji białka ulega ono degradacji.
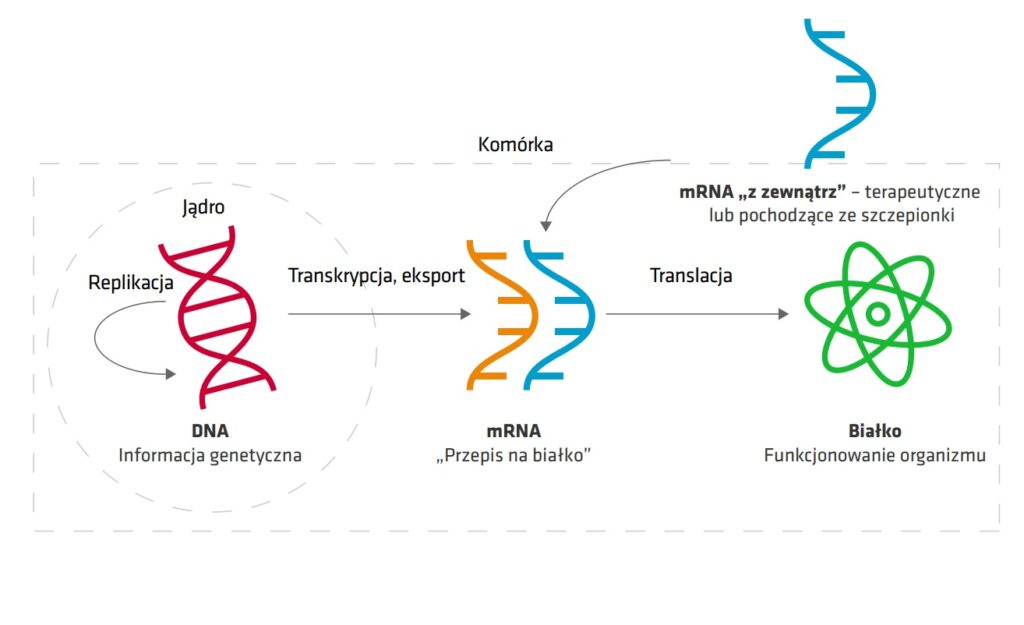
Pomyślmy teraz o mRNA zawartym w szczepionce w tych samych kategoriach (rys. 2). Jest to nic innego, jak tylko „przepis na białko” wirusa SARS-CoV-2, który po wprowadzeniu do naszych komórek pozostaje w cytoplazmie (bo nie potrafi wniknąć do jądra komórkowego), jest „czytany” za pomocą tych samych mechanizmów, które odczytują nasze własne mRNA, a na jego podstawie nasze komórki same tworzą białko lub fragment białka wirusa. Białko to następnie jest uwalniane na zewnętrz komórki i rozpoznawane przez komórki układu odpornościowego jako białko obce i likwidowane w naturalnych procesach immunologicznych. W efekcie organizm niejako uczy się, jak wygląda patogen, i przy kolejnym kontakcie posiada już gotowy arsenał przeciwko niemu czyli, mówiąc prosto, nabiera odporności.
Wykorzystanie cząsteczek mRNA w szczepionce ma zatem kilka ważnych konsekwencji:
- Cząsteczki mRNA są strukturami naturalnie występującym w naszych komórkach. Ponieważ ze szczepionką otrzymujemy mRNA, nie ma możliwości, aby wniknęło ono do jądra komórkowego i zostało przepisane na DNA. Mitem jest zatem to, że szczepienie wpłynie na materiał genetyczny człowieka.
- Cząsteczki mRNA znajdujące się w szczepionce tylko z nazwy są „wirusowe”, ponieważ nie pozyskuje się ich z wirusa, ale powstają w całości w laboratorium za pomocą syntezy chemicznej. Nawet gdyby pochodziły one z zabitych, poszatkowanych wirusów, i tak nie byłyby w stanie wywołać u człowieka infekcji, z uwagi na to, że mRNA zawarte w szczepionce koduje jedynie fragment białka S wirusa, które jest tylko jednym spośród wielu struktur potrzebnych wirusowi do istnienia.
- mRNA jako cząsteczka nietrwała pozostaje w komórkach bardzo krótko (godziny), następnie jest degradowane do nieszkodliwych, naturalnych składników, jakimi są nukleotydy. W konsekwencji w komórkach pozostają jedynie białka, które zostały zsyntetyzowane dokładnie tak, jak wszystkie inne białka zaszczepione-go człowieka. Nie mają one zatem znaczników charakterystycznych dla obcych białek, więc powinny być le-piej tolerowane.
- Produkcja szczepionek mRNA jest stosunkowo łatwa. Zatem jeśli pojawią się nowe warianty wirusa, przeciw którym obecne na rynku szczepionki będą nieskuteczne, w krótkim czasie możliwe będzie zsyntetyzowanie w laboratorium różnych wariantów mRNA, kodujących różne warianty białka kolca, i umieszczenie ich w kolejnych wersjach szczepionki.
- Nietrwałość cząstki mRNA ma też, niestety, negatywne konsekwencje w postaci konieczności transportu i przechowywania szczepionki w bardzo niskich temperaturach oraz krótkiego czasu przydatności do użycia po rozmrożeniu, co znacznie utrudnia logistykę szczepień populacyjnych.
Wykorzystanie mRNA w terapii chorób oraz w szczepieniach nie jest nowym pomysłem. Ostatnie 20 lat było czasem intensywnych prac nad rozwojem terapeutycznych cząsteczek mRNA, których owocem był szereg odkryć pozwalających na osiągnięcie lepszej ich trwałości, zmniejszenia immunogenności oraz rozwiązania problemów z wprowadzeniem mRNA do komórek.
Szczepionki wektorowe
W ostatnim czasie proces warunkowej rejestracji przeszła kolejna szczepionka, tzw. wektorowa – COVID-19 Vaccine AstraZeneca. Zasada działania szczepionki wektorowej jest taka sama, jak w przypadku opisanych wcześniej szczepionek. Tu również do komórek człowieka wprowadzona zostaje informacja, na podstawie której powstaje białko kolca wirusa SARS-CoV-2, które wywołuje odpowiedź immunologiczną. Tym, co odróżnia szczepionki wektorowe od wcześniej opisanych preparatów, jest sposób, w jaki ta informacja zostaje za-pisana i wprowadzona do komórki (rys. 3).
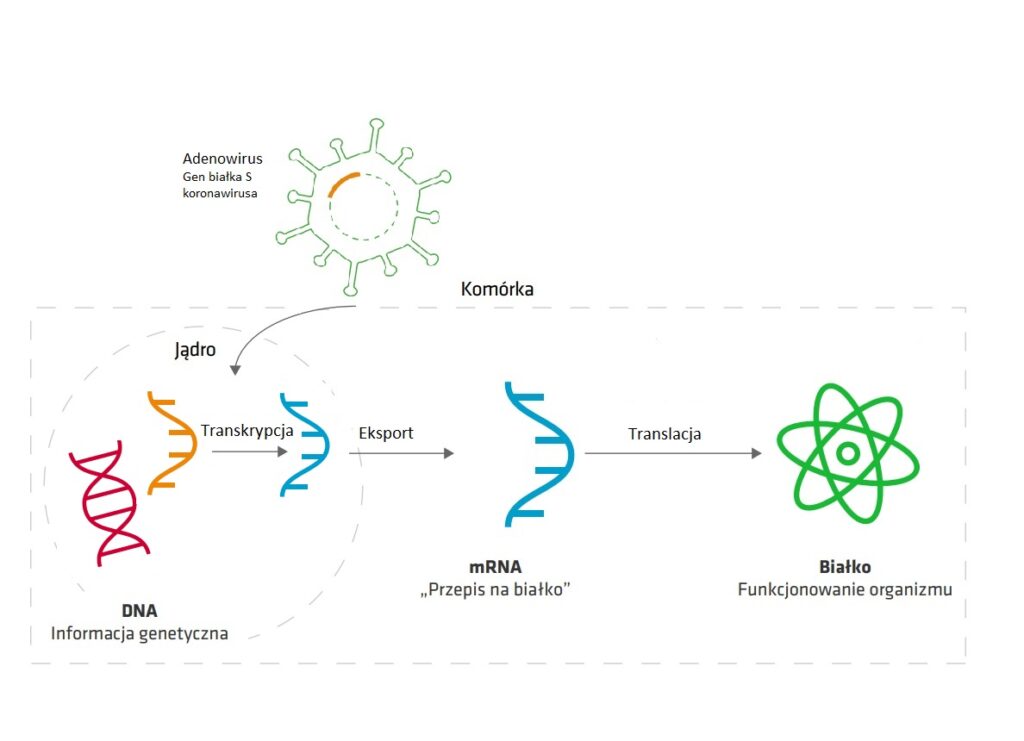
W szczepionce wektorowej wykorzystuje się niegroźne dla człowieka wirusy występujące naturalnie w przyrodzie. W szczepionce firmy AstraZeneca wykorzystano adenowirusa szympansiego, który nie jest zdolny do wywołania infekcji u ludzi. Dla bezpieczeństwa został on dodatkowo zmieniony tak, że nie byłby w stanie wywołać infekcji u nikogo, nawet u szympansa. Adenowirusy są DNA-wirusami, co oznacza, że ich materiał genetyczny stanowi DNA. Szczepionka wektorowa firmy AstraZeneca została stworzona poprzez wprowadzenie sekwencji białka S wirusa SARS-CoV-2 do genomu (materiału genetycznego) adenowirusa. Taki zmodyfikowany adenowirus wnika do cytoplazmy komórek, a następnie wprowadza swój materiał genetyczny do jądra komórkowego, gdzie ulega on naturalnej transkrypcji, czyli przepisaniu na cząsteczkę mRNA. Powstała nić mRNA z jądra komórkowego transportowana zostaje do cytoplazmy komórki, gdzie na jej podstawie produkowane jest białko S prowokujące odpowiedź immunologiczną. Warto wspomnieć, że adenowirus zastosowany w szczepionce, choć wnika do jądra komórkowego, nie ma zdolności integracji swojego materiału genetycznego z DNA człowieka, a więc także w przypadku tej szczepionki nasz materiał genetyczny jest bezpieczny. Dzięki zastosowaniu wektora wirusowego, szczepionka COVID-19 Vaccine Astra-Zeneca wymaga mniej rygorystycznych warunków przechowywania i transportu, co przekłada się na łatwiejszą logistykę szczepień populacyjnych. W badaniach klinicznych prowadzonych przed rejestracją stwierdzono relatywnie gorszą skuteczność szczepionki w porównaniu do szczepionek mRNA (ok. 60% po podaniu dwóch dawek szczepionki), ale należy zauważyć, że przebieg choroby u osób zaszczepionych był na tyle łagodny, że żadna z nich nie wymagała hospitalizacji. Jednak według danych zebranych po dopuszczeniu szczepionki do obrotu, opublikowanych na początku lutego 2021 r., skuteczność szczepionki COVID-19 Vaccine Astra-Zeneca oceniono na 76%, a nawet 82% przy wydłużeniu odstępu między dawkami do 3 miesięcy.
W fazie badań klinicznych jest aktualnie kilka kolejnych szczepionek wektorowych, a także kilka szczepionek tzw. rekombinowanych (zawierających po prostu gotowe białko kolca, które po wprowadzeniu do organizmu człowieka wywołać ma odpowiedź immunologiczną) i inaktywowanych (zwierających wirusa SARS-CoV-2 niezdolnego do wywołania infekcji). Szczepionki, na które Polska zawarła umowy na zakup, przedstawiono w tab. 1.
| Szczepionka | Rodzaj | Liczba dawek | Odstęp | Liczba zakupionych lub zamówionych dawek |
|---|---|---|---|---|
| AstraZeneca | wektorowa | 2 | 4 tygodnie | 16 mln |
| Jonhson&Johnson | wektorowa | 1 | – | 16 980 000 |
| Novavax | podjednostkowa | 2 | 3 tygodnie | 8 371 045 |
| Valneva | inaktywowana | 2 | 3 tygodnie | 10 000 |
| Moderna | mRNA | 2 | 4 tygodnie | 10 881 843 |
| Pfizer/BioNTech | mRNA | 2 | 3 tygodnie | 41 739 871 |
| CureVac | mRNa | 2 | 4 tygodnie | 5 649 979 |
Niepożądane odczyny poszczepienne
Szczepionki są bardzo bezpieczną for-mą ochrony przed infekcjami, niestety, jak każda substancja podawana człowiekowi, mogą wywołać działania niepożądane, zwane w przypadku szczepionek niepożądanymi odczynami poszczepiennymi (NOP). Z dotychczas przeprowadzonych badań klinicznych i doniesień po rozpoczęciu szczepień populacyjnych wynika, że niepożądane odczyny poszczepienne były dość częste, ale miały przeważnie charakter łagodny lub umiarkowany i trwały ok. 1–3 dni. Najczęściej zgłaszane były objawy miejscowe takie jak ból, przekrwienie, zaczerwienienie w miejscu wkłucia i objawy uogólnione, takie jak uczucie rozbicia, dreszcze, bóle mięśniowe, rzadziej stany podgorączkowe czy gorączka. Są to objawy toczącego się stanu zapalnego, znacznie łagodniejsze i trwające krócej niż w przypadku zachorowania na COVID-19. Przewrotnie można by więc stwierdzić, że dolegliwości te, jeśli są łagodne, należałoby po prostu potraktować jako spodziewaną, fizjologiczną reakcję układu odpornościowego na szczepionkę.
Przeciwwskazania do szczepień
Zgodnie z obecną wiedzą medyczną, jedynym bezwzględnym przeciwwskazaniem do szczepienia przeciwko CO-VID-19 jest ogólnoustrojowa reakcja anafilaktyczna (ciężka, zagrażająca życiu reakcja alergiczna) po pierwszej dawce szczepionki lub przebyta ogólnoustrojowa reakcja anafilaktyczna na substancje wchodzące w skład szczepionki. Należy zachować szczególną ostrożność przy szczepieniu osób, u których w przeszłości wystąpiła reakcja anafilaktyczna na inną substancję niż te zawarte w szczepionce. Takie osoby mogą zostać warunkowo zaszczepione przy pełnym zabezpieczeniu przeciwwstrząsowym w warunkach szpitalnych.
Przeciwwskazaniem czasowym do szczepienia jest ostra infekcja przebiegająca z gorączką, zaostrzenie choroby przewlekłej (u chorych na mukowiscydozę zaostrzenie choroby oskrzelowo-płucnej), a także aktywne zakażenie wirusem SARS-CoV-2. Mogą być natomiast szczepieni chorzy, którzy przewlekle przyjmują antybiotykoterapię doustną lub wziewną.
Szczepienia u ozdrowieńców
Ponieważ COVID-19 to nowa choro-ba, z uwagi na krótki okres obserwacji, trudno jest na razie określić, jak długo utrzymuje się odporność po przechorowaniu. Ukazały się do tej pory pojedyncze doniesienia o ponownych zachorowaniach. Z tego względu należy rozważyć szczepienie przeciwko wirusowi SARS-CoV-2 także u osób, które przechorowały COVID-19. Według aktualnych rekomendacji powinno być ono wykonane nie wcześniej niż po 30 dniach od zakończenia infekcji, ale w ciągu 3 miesięcy od zachorowania. U osób, które otrzymały w trakcie choroby osocze ozdrowieńców, szczepienie należy wykonać nie wcześniej niż po 90 dniach od jego przetoczenia.
Szczepienia w grupach ryzyka
Dość liczną grupę chorych na mukowiscydozę stanowią biorcy narządów. U osób tych konieczne jest stosowanie leczenia immunosupresyjnego. Warto wspomnieć, że szczepienie przeciwko COVID-19 powinno się wykonać (podobnie jak inne szczepienia) przed przeszczepieniem narządu, a jeśli to niemożliwe, wskazane jest odroczenie szczepienia przez 6 miesięcy po operacji.
Chorzy, którzy przyjmują przewlekle glikokortykosteroidy doustne lub wziewne, także mogą zostać zaszczepieni. Niestety, trzeba zwrócić uwagę na to, że zarówno leczenie immunomodulujące stosowane po przeszczepieniu narządów, jak i przewlekła steroidoterapia mogą obniżyć skuteczność szczepionki. Jednak potencjalnie mniejsza skuteczność szczepionki u tych chorych nie powinna być powodem zaniechania szczepienia. Nie należy także odstawiać leków immunomodulujących ani glikokortykosteroidów ze względu na szczepienie.
U chorych, u których w przebiegu mukowiscydozy wystąpiły poważne zaburzenia krzepnięcia krwi (małopłytkowość, niewydolność wątroby) ze względu na zwiększone ryzyko wystąpienia wynaczynień krwi i krwawień wskazane jest wyrównanie niedoborów przed szczepieniem (jeśli jest ono możliwe) oraz stosowanie ucisku w miejscu wkłucia.
Ponieważ w badaniach klinicznych nad dostępnymi obecnie na rynku szczepionkami przeciwko COVID-19 nie brały udziału kobiety ciężarne i karmiące piersią, nie ma jednoznacznych danych odnośnie bezpieczeństwa wykonywania szczepień w tych grupach kobiet, nie ma jednak również danych sugerujących, że szczepienie to powinno być u nich przeciwwskazane. W przedklinicznych badaniach toksyczności rozwojowej i reprodukcyjnej (Developmental Reproductive Toxity – DART) przeprowadzonych na modelach zwierzęcych nie zaobserwowano żadnych niepokojących sygnałów dotyczących bezpieczeństwa w tym obszarze. Dostępne dane wskazują, że kobiety w ciąży należą do grupy ryzyka ciężkie-go przebiegu COVID-19, zwłaszcza jeśli mają choroby współistniejące, takie jak otyłość czy cukrzyca. W związku z tym, zgodnie z zaleceniami Amerykańskiego Kolegium Położników i Ginekologów (American College of Obstetricians and Gynecologists), nie można odmówić kobiecie ciężarnej szczepienia, jeśli podejmie decyzję, że chciałaby je otrzymać. Szczepienie jest rekomendowane dla kobiet starających się zajść w ciążę, nie ma konieczności opóźniania zajścia w ciążę po szczepieniu przeciwko COVID-19. Kobietom w okresie laktacji także rekomenduje się szczepienie, a po otrzymaniu szczepionki nie trzeba przerywać karmienia piersią.
Podsumowując, wydaje się, że szczepionki mogą być tym długo wyczekiwanym remedium, które pozwoli za-kończyć pandemię i powrócić do przedpandemicznej normalności. Wymaga to jednak zbudowania tzw. odporności populacyjnej, która jest możliwa, tylko gdy zdecydowana większość społeczeństwa posiada odporność. W takiej populacji zablokowane są kanały transmisji, co oznacza, że wirus nie mogąc się swobodnie przenosić z człowieka na człowieka, prawdopodobnie nie dotrze do osób nieuodpornionych. Dzieje się tak, ponieważ wirus po przeniesieniu się na kolejną osobę, już na początku infekcji natrafia na przygotowane mechanizmy obronne i zostaje ona niejako „zduszona w zarodku”. Taka osoba nie tylko sama nie rozwinie objawów zakażenia, ale też nie będzie przekazywać wirusa dalej. W efekcie chronione są nie tylko osoby zaszczepione, a więc odporne, ale także te, które z różnych przyczyn nie otrzyma-ły szczepienia.
Bibliografia
- Anderson E.J., Rouphael N.G., Widge A.T. i in. Safety and Immunogenicity of SARS-CoV-2 mRNA-1273 Vaccine in Older Adults. N Engl J Med 2020; 383: s. 2427–2438.
- Baden L.R., Sahly H.M., Essink B. i in. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. December 30, 2020, doi: 10.1056/NEJ-Moa2035389
- Charakterystyka produktu leczniczego Co-mirnaty Pfizer BioNTech.
- Charakterystyka produktu leczniczego CO-VID-19 Vaccine AstraZeneca.
- Charakterystyka produktu leczniczego Mo-derna COVID-19 Vaccine.
- COVID-CF project in Europe, European Cystic Fibrosis Society Patient Registry (20.01.2021)
- Fal M. Ali in. Szczepienia przeciwko COVID-19. Innowacyjne technologie i efektywność, Nauka przeciw pandemii (2.02.2021).
- Jackson L.A., Anderson E.J., Rouphael N.G. i in. An mRNA Vaccine against SARS-CoV-2 –Preliminary Report. N Engl J Med 2020; 383: s. 1920–1931.
- Polack F.P., Thomas S.J., Kitchin N. i in. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. N Engl J Med 2020; 383: s. 2603–2615.
- Rekomendacje Zespołu Ekspertów pod kierunkiem Konsultanta Krajowego w dziedzinie Alergologii dotyczące szczepienia przeciwko COVID-19 szczepionką mRNA (Comirnaty) dla Lekarzy kwalifikujących do szczepienia i dla Konsultantów Alergologów (28.12.2020).
- Stanowisko Głównego Polskiego Towarzystwa Epidemiologów i Lekarzy Chorób Zakaźnych w sprawie najczęstszych wątpliwości dotyczących szczepienia przeciw SARS-CoV-2 (26.01.2021).
- Stanowisko Polskiego Towarzystwa Mukowiscydozy, www.pcfs.pl
- Stanowisko Zarządu Głównego Polskiego Towarzystwa Reumatologicznego i konsultanta krajowego w dziedzinie reumatologii dotyczące szczepień przeciwko COVID-19 u pacjentów z autoimmunologicznymi i zapalnymi chorobami reumatycznymi (12.01.2021).
- The Advisory Committee on Immunization Practices (ACIP) recommendations for the use of Pfizer-BioNTech and Moderna COV-ID-19 vaccines for the prevention of coronavirus disease 2019 (COVID-19) in the United States (21.01.2021).
- United Kingdom Cystic Fibrosis Medical Association’s statement on coronavirus, Update on COVID-19 guidance (11.01.2021).
- Vaccinating Pregnant and Lactating Patients Against COVID-19, American College of Obstetricians and Gynecologists (4.02.2021).
- Voysey M., Costa Clemens S.A., Madhi S.A. i in. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet, 2020.
- Wise Jacqui. Covid-19: New data on Oxford AstraZeneca vaccine backs 12 week dosing interval, BMJ 2021; 372:n326.